Permanganato
De Wikipedia, la enciclopedia libre
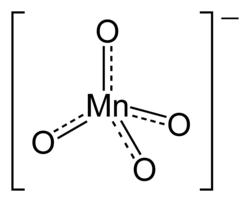
Los permanganatos son las sales del ácido permangánico o permanganésico HMnO4. Se trata de sustancias de un intenso color violeta y alto poder oxidante que contienen el anión MnO4? y por lo tanto el manganeso en su mayor estado de oxidación 7+.
Tabla de contenidos |
[editar] Reacciones
El anión permanganato es tiene un potencial normal de electrodo muy alto, lo que lo convierte en un oxidante muy fuerte capaz de oxidar al agua a oxígeno
4 MnO4– + 4 H+ ? 3 O2 + 2 H2 + 4 MnO2
Sin embargo, esta reacción es muy lenta, sobre todo en ausencia de luz y en medios neutros y alcalinos, lo que hace que esta sustancia sea cinéticamente estable en disolución acuosa.[1] En disolución ácida, aunque lenta, la reducción del permanganto por el agua es observable.[2]
Esta reacción también se puede ver activada aumentando la temperatura. Así, calentando permanganato en disolución alcalina se libera oxígeno elemental y se forman los manganatos con el ion MnO42? y color verde:
4 MnO4? + 4 OH? ? 4 MnO42? + O2 + 2 H2O
En contacto con sustancias orgánicas provocan incendios. Así una gota de glicerina aplicada a un cono de 2-3 g de permanganato de potasio en polvo lleva rápidamente primero a generación de humo y luego a una llama violácea por la presencia del potásio.
En disolución ácida su reducción suele llegar hasta el manganeso (2+), un ion casi incoloro. La reacción es acelerada por la presencia de iones de manganeso (II) (reacción autocatalítica) y aprovechada en la permanganometría.
En disolución neutra o ligeramente básica la reducción sólo lleva hacia el óxido de manganeso (IV), MnO2, que precipita como sólido marrón.[2]
En disoluciones fuertemente alcalinas, el MnO4– se reduce hasta manganeso (VI) en forma de manganato, de color verde[1]
2 MnO4? + H2O2 + 2 OH– ? 2 MnO42- + O2 + 2 H“O
Sin embargo, con un exceso de una sustancia de gran poder reductor, incluso en medios fuertemente básicos se consigue la reducción hasta Mn(IV):
2 MnO4? + 3 SO32? + H2O ? 2 MnO2 + SO42- + 2 OH–
El manganato, estable en disolución altamente alcalina, dismuta cuando se acidifica la disolución para dar manganeso en estados de oxidación (VII) y (IV)[1]
3 MnO42? + 4 H+ ? 2MnO4– + MnO2 + 2 H2O
[editar] Síntesis
El permanganato más conocido es el permanganato potásico KMnO4. Se obtiene mediante electrólisis o por dismutación de una disolución de manganato potásico (K2MnO4) en medio ácido.
[editar] Aplicaciones
El permanganato potásico se utiliza como oxidante en diversos procesos técnicos. Por ejemplo se aprovecha para oxidar el grupo metilo del ácido o-metilclorosulfónico a carboxilato en la síntesis de la sacarina.
En el tratamiento de las aguas residuales a veces se añade permanganato como desinfectante, oxidante y para ayudar a la floculación.
En medicina se utiliza a veces una disolución diluida como desinfectante bucal o dermal.
[editar] Consejos
Las manchas generadas por el permanganato suelen ser debido a la formación de óxidos de manganeso y se eliminan fácilmente con disoluciones ligeramente aciduladas de sulfito o tiosulfato.
[editar] Teoría
El color violeta intenso se debe a una transferencia de carga de entre los oxígenos y el átomo de manganeso central.
El ácido oxálico es un reductor de permanganato y neutralizante de las oxidos de manganeso que generan manchas.
[editar] Referencias
- ? a b c F. Burriel, F. Lucena, S. Arribas, J. Hernández (2006) Química Analítica Cualitativa, 18ª Edición (4ª reimpresión), Madrid, Paraninfo, ISBN 84-9732-140-5
- ? a b F. A. Cotton, G. Wilkinson, C. A. Murillo, y M. Bochmann (1999). “Advanced Inorganic Chemistry”, 6ª Edición. Wiley-VCH. ISBN 0-471-19957-5