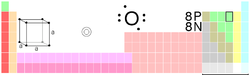
Oxígeno
De Wikipedia, la enciclopedia libre
- Este artículo trata sobre el elemento atómico (O). Para el compuesto químico O2, formado por dos átomos de este elemento, véase Dioxígeno. Para otros usos de este término véase Oxígeno (desambiguación).
|
|||||||||||||||||||||||||
| General | |||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Nombre, símbolo, número | Oxígeno, O, 8 | ||||||||||||||||||||||||
| Serie química | no metal | ||||||||||||||||||||||||
| Grupo, periodo, bloque | 16, 2 , p | ||||||||||||||||||||||||
| Densidad, dureza Mohs | 1,429 kg/m3 (273K), SD | ||||||||||||||||||||||||
| Apariencia | Incoloro |
||||||||||||||||||||||||
| Propiedades atómicas | |||||||||||||||||||||||||
| Masa atómica | 15,9994 u | ||||||||||||||||||||||||
| Radio atómico calculado | 60 (48) pm | ||||||||||||||||||||||||
| Radio covalente | 73 pm | ||||||||||||||||||||||||
| Radio de Van der Waals | 152 pm | ||||||||||||||||||||||||
| Configuración electrónica | [He]2s22p4 | ||||||||||||||||||||||||
| Estados de oxidación (Óxido) | -2,-1 (neutro) | ||||||||||||||||||||||||
| Estructura cristalina | cubic | ||||||||||||||||||||||||
| Propiedades físicas | |||||||||||||||||||||||||
| Estado de la materia | gas (paramagnético) | ||||||||||||||||||||||||
| Punto de fusión | 50,35 K | ||||||||||||||||||||||||
| Punto de ebullición | 90,18 K | ||||||||||||||||||||||||
| Entalpía de vaporización | 3,4099 kJ/mol | ||||||||||||||||||||||||
| Entalpía de fusión | 0,22259 kJ/mol | ||||||||||||||||||||||||
| Presión de vapor | __ Pa a __ K | ||||||||||||||||||||||||
| Velocidad del sonido | 317,5 m/s a 293 K | ||||||||||||||||||||||||
| Información diversa | |||||||||||||||||||||||||
| Electronegatividad | 3,44 (Pauling) | ||||||||||||||||||||||||
| Calor específico | 920 J/(kg*K) | ||||||||||||||||||||||||
| Conductividad eléctrica | _ m-1·?-1 | ||||||||||||||||||||||||
| Conductividad térmica | 0,02674 W/(m*K) | ||||||||||||||||||||||||
| 1° potencial de ionización | 1313,9 kJ/mol | ||||||||||||||||||||||||
| 2° potencial de ionización | 3388,3 kJ/mol | ||||||||||||||||||||||||
| 3° potencial de ionización | 5300,5 kJ/mol | ||||||||||||||||||||||||
| 4° potencial de ionización | 7469,2 kJ/mol | ||||||||||||||||||||||||
| Isótopos más estables | |||||||||||||||||||||||||
|
|||||||||||||||||||||||||
| Valores en el SI y en condiciones normales (0 °C y 1 atm), salvo que se indique lo contrario. ?Calculado a partir de distintas longitudes de enlace covalente, metálico o iónico. |
|||||||||||||||||||||||||

Por una coincidencia interesante de la naturaleza, el oxígeno líquido tiene el color celeste del cielo. Es importante observar que sin embargo, estos dos fenómenos no tienen relación (el azul del cielo es debido a la dispersión de Rayleigh y estaría presente aunque no hubiese oxígeno en el aire).
El oxígeno es un elemento químico de número atómico 8 y símbolo O. En su forma molecular más frecuente, O2, es un gas a temperatura ambiente. Representa aproximadamente el 21% en volumen de la composición de la atmósfera terrestre. Es uno de los elementos más importantes de la química orgánica y participa de forma muy importante en el ciclo energético de los seres vivos, esencial en la respiración celular de los organismos aeróbicos. Es un gas incoloro, inodoro (sin olor) e insípido. Existe una forma molecular formada por tres átomos de oxígeno, O3, denominada ozono cuya presencia en la atmósfera protege la Tierra de la incidencia de radiación ultravioleta procedente del Sol.
Un átomo de oxígeno combinado con dos de hidrógeno forman una molécula de agua.
Tabla de contenidos |
[editar] Características principales
En condiciones normales de presión y temperatura, el oxígeno se encuentra en estado gaseoso formando moléculas diatómicas (O2) que a pesar de ser inestables se generan durante la fotosíntesis de las plantas y son posteriormente utilizadas por los animales, en la respiración (ver ciclo del oxígeno). También se puede encontrar de forma líquida en laboratorios. Si llega a una temperatura menor que -219°C, se convierte en un sólido cristalino azul su valencia es 2.
[editar] Descubrimiento
Carl Wilhelm Scheele (1742-1786) farmacéutico y químico sueco (aunque de origen alemán), describe el descubrimiento del oxígeno, producido durante sus trabajos entre 1772 y 1773, en su libro Chemische Abhandlung von der Luft und dem Feuer (Tratado químico del aire y del fuego) publicado en 1777.
Tradicionalmente este descubrimiento ha sido atribuido al químico angloamericano Joseph Priestley (1733-1804), quien lo descubrió de manera independiente en 1772, aunque el primero que publicó un trabajo sobre este gas y le dio nombre fue el químico francés Lavoisier (1743-1794) en 1777. Utilizó para ello dos raíces griegas ???? (oxýs) (ácido, literalmente “punzante”, por el sabor de los ácidos) y –????? (-gen?s) (“generador, que engendra”), porque creyó que el oxígeno era un constituyente indispensable de los ácidos).
Al calentar monóxido de mercurio, Priestley obtuvo dos vapores: uno se condensó en gotitas, el mercurio, pero ¿qué era el otro? Priestley juntó ese gas en un recipiente e hizo algunos ensayos: si introducía una brasa de madera, ardía; si acercaba ratones vivos, éstos se volvían muy activos. En vista de lo cual, Priestley inhaló un poco de ese gas y notó que se sentía muy “ligero y cómodo”. A este gas lo llamó aire desflogistizado, hoy sabemos que era oxígeno. Sin saberlo, Priestley fue la primera persona que usó la mascarilla de oxígeno.
[editar] Rol biológico
El oxígeno respirado por los organismos aerobios, liberado por la plantas mediante la fotosíntesis, participa en la conversión de nutrientes en energía (ATP). Su disminución provoca hipoxemia y la falta total de él anoxia pudiendo provocar la muerte del organismo.
[editar] Isótopos
El oxígeno tiene tres isótopos estables y diez radioactivos. Todos sus isótopos radioactivos tienen un periodo de semidesintegración de menos de tres minutos.
[editar] Iones Típicos
El oxígeno puede formas gran variedad de de iones y estados de oxidación distintos
-
- Oxido, O12? estado de oxidación -2
- Peróxido, O22? estado de oxidación -1
- Superóxido, O2? estado de oxidación -1/2
- Ozónido, O3? estado de oxidación -1/3
Combinaciones con el Fluor, únicas con oxigeno en estado de oxidación postitivo
FOOF F2O2 Estado de oxidación +1
FOF F2O1 Estado de oxidación +2
[editar] Precauciones
El oxígeno puede ser tóxico a elevadas presiones parciales.
Algunos compuestos como el ozono, el peróxido de hidrógeno y radicales hidroxilo son muy tóxicos. El cuerpo humano ha desarrollado mecanismos de protección contra estas especies tóxicas. Por ejemplo la glutation actúa como antioxidante, al igual que la bilirrubina (un producto derivado del metabolismo de la hemoglobina)
[editar] Véase también
- Anoxia;
- Ciclo del oxígeno;
- Oxígeno diatómico o gaseoso;
- Terapia mediante oxígeno.
[editar] Enlaces externos
 Commons alberga contenido multimedia sobre Oxígeno.Commons
Commons alberga contenido multimedia sobre Oxígeno.Commons- Enciclopedia Libre
- Los Alamos National Laboratory – Oxygen
- WebElements.com – Oxygen
- EnvironmentalChemistry.com – Oxygen
- It’s Elemental – Oxygen
- Oxygen Therapy – The First 150 Years
- Oxygen Toxicity